格列卫诞生记:难以复制的抗癌奇迹
格列卫诞生记:难以复制的抗癌奇迹
有人将它称为一个奇迹,也有人把它比作是杀死魔物的银色子弹。自2001年获批问世以来,格列卫(Gleevec,imatinib)在慢性白血病的治疗上取得了傲人的成绩,被誉为是人类抗癌史上的一大突破。
而在最近,随着一部电影的上映,格列卫这个名字,又再次成为了公众热议的话题。
癌症与染色体
让我们先把时钟拨回到100年前。当时的科学家们对癌症知之甚少,主流学界也简单地把癌症归因于病毒感染或是环境因素。但一名叫做西奥多·勃法瑞(Theodor Boveri)的科学家却不这么看。
在动物实验中,一些生理学家发现有丝分裂的异常,会让海胆出现类似于癌症发作的现象。
基于这些观察,西奥多也提出了几个假设:
· 肿瘤细胞的遗传物质也许不稳定
· 肿瘤可能是从单个癌细胞发育而来
· 染色体异常使肿瘤细胞的生长失控
这些导致肿瘤的遗传变化发生在比染色体更小的尺度上,所以我们无法通过显微镜观察。

▲西奥多的假设极富前瞻性(图片来源:See page for author [Public domain], via Wikimedia Commons)
以目前对癌症的理解,我们不难发现,西奥多百年前的假设竟如此富有前瞻性。但他的灵光一闪实在太过超前了——限于科研能力的局限,直到1921年,科学家们还相信人类的基因组里有48条染色体。可以想象,西奥多那不合时宜的天才想法,注定无法得到时代的验证与认可。
几十年后,随着细胞遗传学的兴起,科学家们方才意识到,染色体也许和疾病也有着关联:他们发现,罹患唐氏综合症的患者有3条21号染色体,而特纳氏综合症的患者,其X染色体会出现部分或完全的缺失。
这些病例清楚地证明染色体异常会导致疾病,那癌症是否也是染色体异常的后果呢?
起初,科学家们并没有达成共识。以白血病为例,一些肿瘤学家只是粗略地对它们进行了分析,然后宣布未能找到任何特殊的染色体异常。在1960年,当时一位著名的学者更是在大量分析后断言,在绝大部分的人类肿瘤细胞中,染色体都是正常的。
然而,同年刊登在《科学》杂志上的一篇论文,却给癌症研究领域带来了一场地震。

▲短短三段文字,永远改变了人类对白血病的认识(图片来源:CMLeukemia)
费城染色体
1956年,一名叫做彼得·诺维尔(Peter Nowell)的年轻人从海军退役,回到了故乡费城。在那里,他加入了宾夕法尼亚大学病理系,主攻白血病和淋巴瘤的研究。

▲费城染色体的发现者之一彼得·诺维尔教授(图片来源:宾夕法尼亚大学纪念网站)
彼得也想探明染色体与血液癌症之间的关系。和当时的许多研究人员不同,他决定用一种新颖的染色技术标记染色体,好更清楚地看清它们的结构——细胞先在玻璃片上生长到一定阶段,再被泡在水中涨裂。随后,渗入细胞的姬姆萨染液(Giemsa Staining)能使染色体从细胞中显现出来。
“当时我对染色体一窍不通,”彼得在多年后的一次采访中回答为何要观察染色体:“我只是觉得不该把它们弃之一旁。”
人类历史的进程,总会在不经意下得到推动。彼得的好奇心很快带来了收获。没过多久,他与研究生一起发现了一个有趣的现象:在慢性骨髓性白血病(CML)患者的癌细胞中,第22号染色体明显要更短。
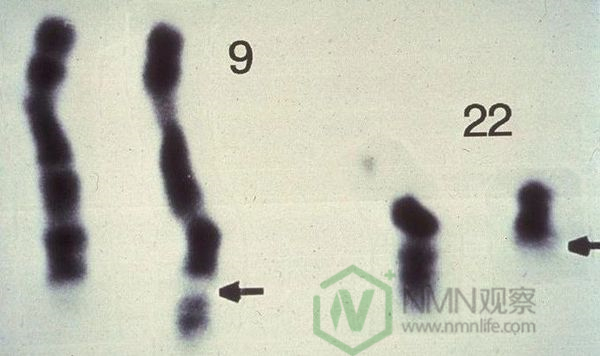
▲一些白血病患者的第22号染色体要明显更短(图片来源:《自然》)
研究人员们敏锐地意识到,这个染色体异常,或许就是此类慢性白血病的潜在病因。后续研究中,研究人员们进一步观察了7名白血病患者的染色体,每一名都带有短小的22号染色体。在接下来的几年中,彼得和他的同事们接连发表多篇论文,向全世界宣告他们的发现。
“每一个典型的病例,每一个细胞都带有这个变异,”彼得说道:“对我来说,这意味着两点。首先,这个遗传变异对这一类型的癌症发作至关重要;其次,这些肿瘤确实是从发生变异的单个细胞生长而来。”
整个癌症研究领域为之震动!
为了表彰宾夕法尼亚大学做出的这一重要发现,患者体内异常的22号染色体也被命名为“费城染色体”。2016年的圣诞节次日,88岁的彼得迎来了生命的终点。在费城近郊出生,也在费城近郊辞世。因为彼得,那座离他只有几十英里的城,永远在人类的抗癌史上留下了自己的名字。
寻找致癌的原因
费城染色体的发现是白血病研究领域的一个重要突破,但却不是终点。相反,它连新药研发道路上迈出的第一步都算不上。光靠染色体异常这一现象,我们依然不知道背后的致病机理。如果我们连疾病的根源都没搞清,又要如何去治疗它呢?
1973年,芝加哥大学的珍妮特·罗利(Janet Rowley)教授在彼得的发现基础上,又前进了一层。她的团队发现,费城染色体之所以短,是因为发生了染色体的易位——人类的9号染色体与22号染色体发生了一部分的交换,让22号染色体短上那么一截。
她敏锐地指出,这个特殊的易位背后,一定存在着某种特殊的致癌机理。
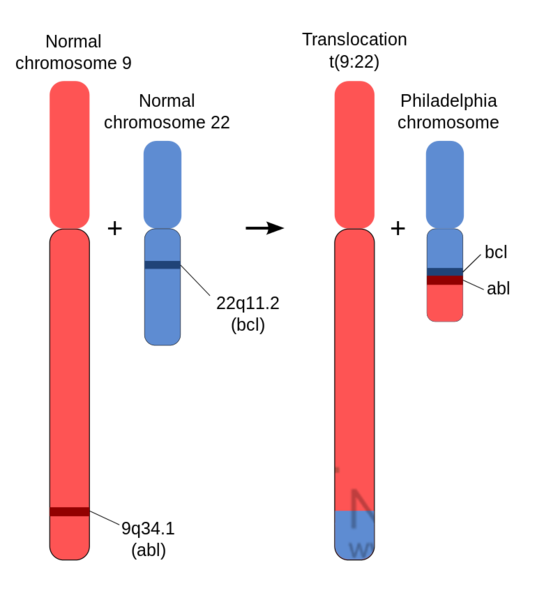
▲费城染色体的致癌原因
为了找到这个致癌机理,我们又等待了10年的时间。
1983年,美国国立癌症研究所(NCI)与Erasmus大学的学者们发现,由于两条染色体之间发生的交错易位,9号染色体上的Abl基因,恰好与22号染色体上的BCR基因连到了一块,产生了一条BCR-Abl融合基因。
这条融合基因编码了一种奇特的酪氨酸激酶。对常规酪氨酸激酶而言,它们的活性受到了严格的控制,不会突然失控;但BCR-Abl蛋白则不同。它不受其他分子的控制,一直处于活跃状态。这就好像是细胞锁死了油门,导致不受控的细胞分裂,引起癌症。
当研究人员们将融合基因导入小鼠的体内后,小鼠果然出现了致命的白血病症状。这个发现也*终证实,BCR与Abl两条基因的融合,是此类白血病的根本原因。
而这一发现距离彼得在1960年发表的论文,已经过去了整整30年。直到这一刻,人类才从未知的领域中探索到了足够多的新知,准备迎接新药研发的挑战。
新药研发的漫漫长路
在上世纪80年代末,CibaGeigy公司(现属于诺华集团)的科学家们启动了一系列寻找蛋白激酶抑制剂的项目。在一个针对蛋白激酶C(PKC)的项目中,研究人员们发现一种2-苯氨基嘧啶(2-phenylamino-pyrimidine)的衍生物展现出了成药的潜力,能同时抑制丝氨酸/苏氨酸激酶与酪氨酸激酶。
尽管这种衍生物的特异性较差,无法直接用于治疗,但它却为新药研发人员们提供了一个研发的起点。
在这个化合物的基础上,研究人员们做了一系列的合成尝试,不断优化这一分子的特性:在嘧啶的3号位上添加的吡啶基团能增加其在细胞内的活性;苯环上添加的苯甲酰胺基团能增强对酪氨酸激酶的抑制能力;苯胺基苯环6号位的修饰进一步增强了对酪氨酸激酶的抑制;N-甲基哌嗪的侧链添加则极大地改善了这个分子的溶解度,使得口服用药成为可能。
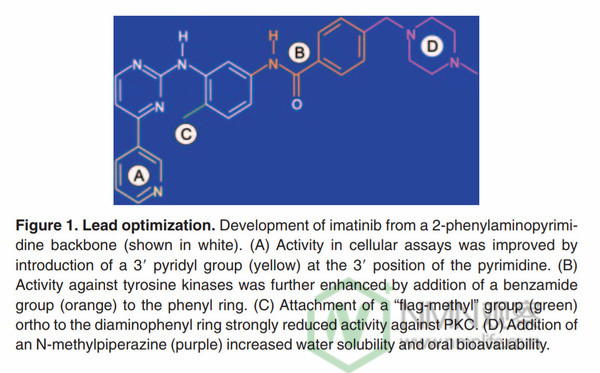
▲新药研发绝非一步登天,其中离不开各种设计与优化
经过一系列的设计与修饰,这款分子彰显出了极高的特异性抑制能力。只要细胞表达BCR-Abl蛋白,其生长就会被这款分子抑制。研究人员相信是时候将它推进到下一阶段了。这款分子的代号是CGP57148B,后来有了一个更为响亮的名字——伊马替尼(imatinib)。
在小鼠实验中,研究人员们进一步优化了这款分子的疗程和剂量。这些小鼠接受了为期11天的治疗,每天使用3次药物。无论是腹腔给药(每公斤体重使用50mg),还是口服给药(每公斤体重使用160mg),在治疗的48个小时后,癌症都得到了明显的控制。
在治疗后的第八天,所有经过治疗的小鼠,症状都消失了。有三分之二(8/12)的小鼠在接下来的200天里,都没有出现疾病复发。这些积极数据,也终于将伊马替尼带到了人体试验的门前。
奇迹般的药物
1998年6月,伊马替尼迎来了历史性的一天——它终于进入了人体试验阶段。在这项1期临床试验中,研究人员们的主要目的,是寻找**耐受剂量,探索这款药物的安全性。研究招募了一群经过治疗,但病情依旧严重的患者,并让他们接受每日伊马替尼的口服疗法。
研究表明该药物不但耐受良好,而且有着堪称奇迹般的疗效:接受300mg剂量的54名患者中,有53名出现了血液学上的完全缓解(complete hematologic responses ,CHR)。
这一可喜的结果,迅速将伊马替尼带往了2期临床试验。1999年启动的2期临床试验再次验证了1期试验中观察到的积极疗效。
更为可喜的是,这些疗效看来相当持久:在治疗的一年半后,患者的无进展生存率依然达到了89.2%。基于其出色的治疗效果,美国FDA在2期临床试验后,就加速批准这款新药问世,治疗慢性骨髓性白血病。而这款药物的产品名,就是我们所熟知的格列卫。
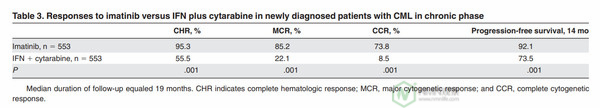
▲3期临床中,格列卫的效果完胜标准疗法
获批之后,研究人员们完成了3期临床试验的工作。相比标准疗法,它在所有指标上都彰显出了显著的疗效。
在格列卫诞生前,只有30%的慢性骨髓性白血病患者能在确诊后活过5年。格列卫将这一数字从30%提高到了89%,且在5年后,依旧有98%的患者取得了血液学上的完全缓解。
为此,它也被列入了世界卫生组织的基本药物标准清单,被认为是医疗系统中“最为有效、最为安全,满足最重大需求”的基本药物之一。
后记 [关注“NMN观察”,获取权威长寿资讯]
从某种意义上说,格列卫是一个不折不扣的奇迹。这不仅因为它不可思议的疗效,还因为它的成功难以复制。与其他癌症不同,慢性骨髓性白血病有着单一的病因。因此,仅仅是一款靶向药物,就能起到极好的效果。
但即便如此,从费城染色体的发现,到美国FDA的加速批准,中间依旧间隔了41年。新药研发之不易,由此也可见一斑。毫无疑问,格列卫的研发故事是科学转化的最佳案例,也掀开了靶向治疗癌症的新篇章。
观察君倡导:在抗癌创新疗法层出不穷的当下,我们也不应忘记,正是这些钻研基础科学的生物学家,以及推动新药问世的研发人员数十年如一日的坚守,才让拯救生命的创新药物成为可能。在这里,我们也向他们致以崇高的敬意!

